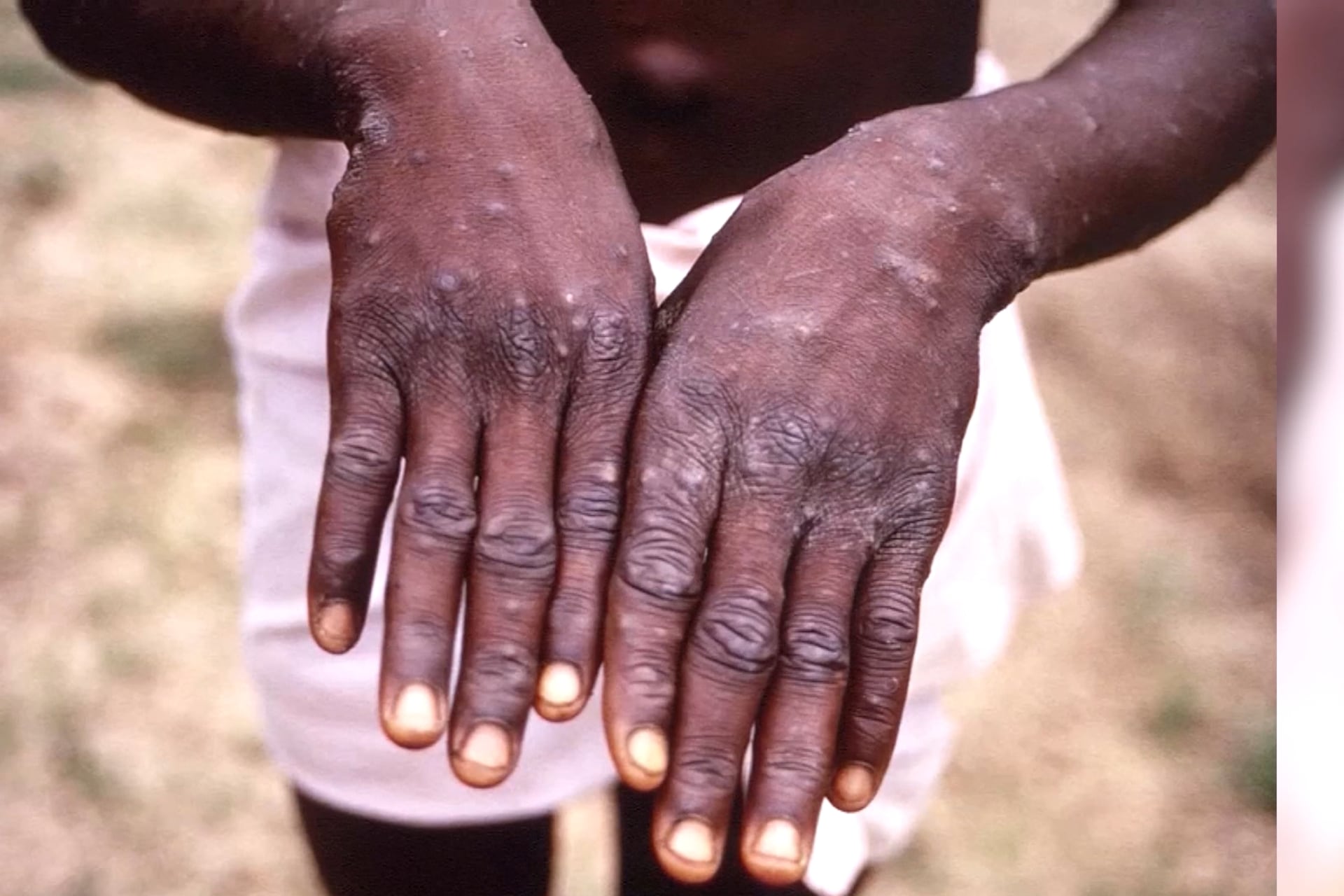
A gripe aviária está infectando milhares de mamíferos: como isso nos ameaça?
Somente em uma colônia de animais marinhos, o vírus matou 17.400 filhotes de foca, mais de 95% dos jovens
Saúde|Apoorva Mandavilli e Emily Anthes, do The New York Times

Em suas três décadas trabalhando com elefantes-marinhos, a dra. Marcela Uhart nunca tinha visto nada parecido com aquela cena nas praias da Península Valdés, na Argentina, em outubro passado.
Era o pico da temporada de reprodução; a praia deveria estar repleta de haréns de fêmeas férteis e machos enormes lutando uns contra os outros pelo domínio da colônia. Em vez disso, havia apenas “carcaças, uma sobre a outra”, lembrou Uhart, diretora do programa de saúde da vida selvagem da América Latina na Universidade da Califórnia, em Davis.
Veja também
O H5N1, um dos muitos vírus que causam a gripe aviária, já havia matado pelo menos 24 mil leões-marinhos sul-americanos ao longo das costas do continente em menos de um ano. Agora, era a vez dos elefantes-marinhos.
Filhotes de todas as idades, desde recém-nascidos até os totalmente desmamados, jaziam mortos ou moribundos na linha da maré alta. Os filhotes doentes estavam apáticos, com espuma escorrendo da boca e do nariz. Uhart classificou a cena como “uma visão do inferno”.
Nas semanas que se seguiram, ela e um colega, protegidos da cabeça aos pés com luvas, avental e máscara, e se encharcando periodicamente com alvejante, documentaram cuidadosamente a devastação. Os membros da equipe ficaram no topo dos penhascos próximos, calculando o número de vítimas com o uso de drones.
A conclusão foi surpreendente: o vírus matou cerca de 17.400 filhotes de foca, mais de 95% dos animais jovens da colônia.
A catástrofe foi a última de uma epidemia de gripe aviária que vem assolando o mundo desde 2020, levando as autoridades de vários continentes a matar milhões de aves, domésticas e de outros tipos. Só nos Estados Unidos, mais de 90 milhões de aves foram abatidas, em uma tentativa inútil de deter o vírus.
Até o momento, nada foi capaz de deter o H5N1. Os vírus da gripe aviária tendem a ser exigentes com relação a seus hospedeiros, geralmente aderindo a um tipo de ave selvagem. Mas esse se infiltrou rapidamente em uma variedade surpreendentemente ampla de aves e animais, desde esquilos e gambás até golfinhos-nariz-de-garrafa, ursos-polares e, mais recentemente, vacas leiteiras.
“Em minha carreira na área de gripe, nunca vimos um vírus que ampliasse sua gama de hospedeiros dessa forma”, declarou Troy Sutton, virologista que estuda os vírus da gripe aviária e humana na Universidade Estadual da Pensilvânia.

O impacto nos mamíferos marinhos e nos setores de laticínios e aves de abate é bastante preocupante. Mas, de acordo com os especialistas, uma preocupação ainda maior é o que vem depois desses desdobramentos: o vírus está se adaptando aos mamíferos e cada vez mais perto de se alastrar entre os humanos.
É absolutamente possível evitar uma pandemia humana. Sutton afirmou que, pelo menos até o momento, as mudanças no vírus não indicam que o H5N1 possa causar uma pandemia. “Ainda assim, não sabemos como interpretar a atual situação ou o que ela significa”, admitiu.
Mortes marinhas
Uma cepa altamente patogênica do H5N1 foi identificada em aves aquáticas domésticas na China em 1996. No ano seguinte, 18 pessoas em Hong Kong foram infectadas com o vírus, e seis delas morreram. Este, em seguida, permaneceu silencioso, mas ressurgiu em Hong Kong em 2003. Desde então, causou dezenas de surtos em aves domésticas e afetou mais de 800 pessoas que estavam em contato próximo com os animais. Durante todo esse período, continuou a evoluir.
A versão do H5N1 em circulação atualmente surgiu na Europa em 2020 e se espalhou rapidamente para a África e a Ásia. Matou dezenas de aves de criação, mas, ao contrário de suas antecessoras, também se espalhou amplamente entre as aves selvagens e muitos outros animais.
A maioria das infecções de mamíferos provavelmente não gerou novos casos: uma raposa que talvez tenha comido uma ave infectada e morreu sem transmitir o vírus. Mas alguns surtos maiores sugeriram que o H5N1 era capaz de fazer mais.
A primeira indicação disso foi no verão de 2022, quando o vírus matou centenas de focas na Nova Inglaterra e na província do Quebec. Alguns meses depois, infiltrou-se em uma fazenda de martas na Espanha.
Pelo menos no caso das martas, a explicação mais provável é que o H5N1 tenha se adaptado para se espalhar entre os animais. A magnitude dos surtos em mamíferos marinhos na América do Sul reforçou essa probabilidade. “Minha tendência é pensar que a transmissão de mamífero para mamífero é muito provável”, disse Malik Peiris, virologista e especialista em gripe aviária da Universidade de Hong Kong.
Depois de ter sido detectado pela primeira vez na América do Sul em outubro de 2022, em aves da Colômbia, o vírus se espalhou pela costa do Pacífico até a Terra do Fogo, extremo sul do continente, e pela costa do Atlântico.
Matou centenas de milhares de aves marinhas e dezenas de milhares de leões-marinhos pelo caminho, no Peru, no Chile, na Argentina, no Uruguai e no Brasil. Os leões-marinhos se comportaram de forma errática, sofrendo convulsões e paralisia; fêmeas grávidas abortaram. “Nunca tínhamos testemunhado o que aconteceu quando o vírus foi para a América do Sul”, comentou Uhart.
Não se sabe exatamente como e quando o vírus passou para os mamíferos marinhos, mas é provável que os leões-marinhos tenham entrado em contato próximo com aves ou fezes contaminadas. (Embora os peixes constituam a maior parte da dieta dos leões-marinhos, esses animais às vezes comem aves.)
Em algum momento, é provável que o vírus tenha evoluído para se disseminar diretamente entre os mamíferos marinhos, já que, na Argentina, as mortes de leões-marinhos não coincidiram com a mortalidade em massa de aves selvagens. “Isso pode sugerir que a fonte de infecção não foram as aves infectadas”, especulou o dr. Pablo Plaza, veterinário de vida selvagem da Universidade Nacional de Comahue e do Conselho Nacional de Pesquisa Científica e Técnica da Argentina.
Não é difícil imaginar como o vírus pode se propagar entre esses animais. Tanto os elefantes quanto os leões-marinhos se reproduzem em colônias, aglomerando-se nas praias onde lutam, acasalam e ladram uns para os outros. Os elefantes-marinhos espirram o dia todo, dispersando grandes gotículas de muco a cada vez que o fazem.
É difícil determinar exatamente como e quando o vírus passou de uma espécie para outra. Mas a análise genética apoia a teoria de que os mamíferos marinhos contraíram a infecção uns dos outros, e não das aves. Amostras isoladas de vírus de leões-marinhos, no Peru e no Chile, e de elefantes marinhos na Argentina compartilham cerca de 15 mutações não observadas nas aves; as mesmas mutações também estavam presentes em um homem chileno infectado no ano passado.
Há inúmeras oportunidades para que o H5N1 seja transmitido dos mamíferos marinhos para as pessoas. Foi constatado que um elefante-marinho macho doente que ficou sentado por um dia e meio em uma praia pública na Argentina carregava enormes quantidades de vírus. No Peru, os cientistas coletaram amostras de carcaças de leões-marinhos que estavam ao lado de famílias que apreciavam um dia na praia.
Animais necrófagos, como cães, também podem contrair o vírus de uma carcaça infectada e disseminá-lo de forma mais ampla: “Nenhum dos animais selvagens existe de forma isolada”, disse Wendy Puryear, virologista da Universidade Tufts que estudou os surtos de focas na Nova Inglaterra.
Em alguns países da América do Sul, com exceção de algumas carcaças que foram enterradas, o restante permaneceu nas praias, apodrecendo e sendo devorado. “Como é possível se organizar para remover 17 mil cadáveres no meio do nada, em lugares onde não se pode nem levar maquinário, em penhascos enormes?”, questionou Uhart.
Patógeno mutante
Os vírus influenza são hábeis em adquirir novas mutações; quando dois tipos infectam o mesmo animal, podem misturar seu material genético e gerar novas versões.
Não se sabe exatamente como nem quanto o vírus H5N1 mudou desde seu surgimento. Um estudo feito no ano passado mostrou que, depois que entrou nos Estados Unidos, o vírus se misturou rapidamente com outros influenza que circulavam no país, dando origem a várias versões – algumas leves, outras causando sintomas neurológicos graves. “Portanto, depois de 20 anos de recombinação, temos um vírus que, na verdade, se comporta extraordinariamente bem em toda uma variedade de espécies de aves e mamíferos”, disse Vincent Munster, virologista do Instituto Nacional de Alergia e Doenças Infecciosas, que estudou as mutações necessárias para que o H5N1 se adapte às pessoas.
Cada nova espécie que abriga o vírus cria oportunidades para que o H5N1 continue a evoluir e infectar humanos.
E o vírus pode se deparar com mutações que ninguém ainda considerou, permitindo que ultrapasse a barreira das espécies. Foi isso que aconteceu no surto de gripe suína de 2009.
Esse vírus não apresentava as mutações que se pensava serem necessárias para infectar pessoas com facilidade. Em vez disso, “ele tinha essas outras mutações que ninguém conhecia ou imaginava até então”, explicou Louise Moncla, bióloga evolucionária que estuda a gripe aviária na Universidade da Pensilvânia.
Ainda assim, mesmo que o vírus passe para as pessoas, “talvez não tenhamos o nível de mortalidade que realmente nos preocupa. A imunidade preexistente às cepas de gripe sazonal vai fornecer alguma proteção contra doenças graves”, observou Seema Lakdawala, virologista da Universidade Emory.
Próximos passos
Os EUA estão preparados para uma pandemia de gripe, com algumas vacinas e antivirais estocados, mas os esforços para monitorar o vírus podem não o detectar com rapidez suficiente para implantar essas ferramentas. Várias semanas decorreram até que os fazendeiros, e depois as autoridades, percebessem que o H5N1 estava circulando em vacas leiteiras.
O surto em fazendas de gado leiteiro resultou em apenas uma infecção humana leve, mas as fazendas são um terreno fértil para que o vírus passe de uma espécie para outra – do gato para a vaca, desta para o porco e deste para o homem, em qualquer ordem.

Muitos cientistas se preocupam especialmente com os suínos, que são suscetíveis a cepas de gripe humana e aviária, proporcionando a mistura perfeita para que os vírus troquem genes. Os porcos são abatidos quando muito jovens, e as novas gerações, sem exposição prévia à gripe, são particularmente vulneráveis a infecções.
Até o momento, o H5N1 não parece ser capaz de infectar porcos, mas isso pode mudar à medida que o vírus adquire novas mutações.
“Sou o tipo de mãe que nunca deixa os filhos irem a feiras estaduais nem fazendas de animais, principalmente porque sei que, quanto maior o número de interações com os animais, mais aumentam as oportunidades de mutação”, disse Lakdawala.
Se o H5N1 se adaptar às pessoas, as autoridades federais precisarão trabalhar juntas e com suas correspondentes internacionais. O nacionalismo, a concorrência e a burocracia podem retardar a troca de informações que é crucial em um surto em desenvolvimento.
De certa forma, a atual disseminação entre as vacas leiteiras é uma oportunidade de praticar o que tem sido treinado, afirmou Rick Bright, CEO da Bright Global Health, empresa de consultoria que se concentra em melhorar as respostas a emergências de saúde pública. Mas ele acrescentou que o Departamento de Agricultura dos EUA está exigindo apenas testes voluntários das vacas, e não está sendo tão oportuno e transparente com suas observações como deveria.
A dra. Rosemary Sifford, veterinária-chefe do departamento, garantiu que a equipe está trabalhando arduamente para compartilhar informações o mais depressa possível: “Essa é considerada uma doença emergente.”
Em geral, as autoridades governamentais são cautelosas e querem ver mais dados. “Mas, diante da rapidez com que isso pode se espalhar, e dada a doença devastadora que pode causar, se nossos líderes hesitarem e não acionarem os gatilhos certos na hora certa, seremos pegos de surpresa mais uma vez. Se não entrarmos em pânico, mas dermos a ele o devido respeito e dedicação, acredito que podemos lidar com esse vírus”, declarou Bright.
c. 2024 The New York Times Company